公司新闻
-
【干货】设备验收需要做的事情全…
-
设备验收需要做哪些事情 一、预确认(PF) 需要的资料主要有: 1、用户需求文件(URS) 由工艺技术人员和设备技术人员共同起草一份综合了各部门(生产部门、质量部门、设备部门、新产品研发部门等)意见的用户需求文件(URS)。 是设备选型和设计的基本依据,因此需要对生产能力、生产工艺、操作需求、清洁需求、可靠性需…

-
这个您得知道——GMP中电子数据备…
-
1.目的:本规程定义了GMP计算机及自动化系统关于数据备份恢复的基本通用规程。规程涉及了数据的产生,存储和归档,采用独立的物理介质备份机制以避免系统因意外事故,网络中断,病毒恶意攻击,系统或软件参数修改等造成重要数据的丢失。2.范围:本操作规程适用于公司所有GMP计算机和自动化系统的电子数据管理,此类系统用于或为…
-
数据完整性,偏差和车间质量
-
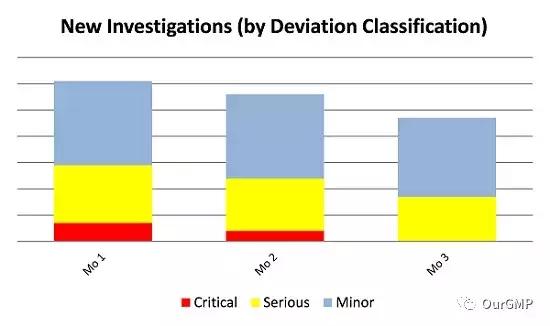
数据完整性的不断提高可以推动企业走向成熟的质量文化,特别是通过在车间实施质量保证。批次记录审核(BRR)和产品配置通常会因数据完整性问题和数据质量差而变得复杂。 BRR和产品配置过程由于生产偏差和质量事件调查而变得更加复杂,增加了必须审查和解决的数据量,以便于产品处置。 ISPEGAMP记录和数据完整性指南(第34页)…
-
「必读」药品生产过程变更控制案…
-
01 引言实施GMP的最根本目的是最大限度的降低药品生产过程中的一系列污染(包括生产过程中的污染、交叉污染、及混淆、差错等风险,)确保持续且稳定生产出符合预定用途和注册要求的药品。同时有效的变更控制系统可以使系统始终处于受控状态,即通过对工艺运行和产品质量的有效监控,为工艺能力及其稳定性提供保障。根据ICH质…

-
「干货」OOS检查重点,OOS调查相…
-
FDA下一阶段更加关注OOS调查FDA药品审评与研究办公室(CDER)国际药品质量处处长CarmeloRosa于去年11月4-7日在费城召开的ISPE年会上表示,随着FDA对制药行业数据可靠性检查的结果开始显现,在其中发现了更多关于超标(OOS)调查的问题。一些公司不再掩盖分析实验室的超标结果,使得最容易出问题之处显露出来。Rosa表示:“现…
-
「干货」GMP中电子数据备份和恢复…
-
1.目的:本规程定义了 GMP 计算机及自动化系统关于数据备份恢复的基本通用规程。规程涉及了数据的产生,存储和归档,采用独立的物理介质备份机制以避免系统因意外事故,网络中断,病毒恶意攻击,系统或软件参数修改等造成重要数据的丢失。2.范围: 本操作规程适用于公司所有GMP计算机和自动化系统的电子数据管理,此类系统用于…



