常见问题
-
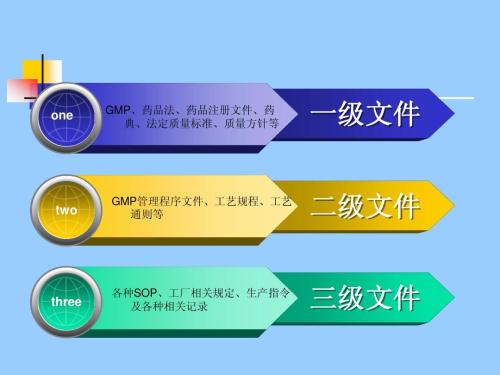
干货:GMP三级文件体系详解
-
1、一级文件:理念性、原则性、纲领性、指导性文件,比如质量方针、验证主计划、工程项目管理规程、厂房设施管理规程、设备管理规程、维护与预防性维护管理规程、计量校准管理规程、变更控制管理规程、偏差管理规程……一级文件就是把法律、法规、规范、指南……的要求,变成公司的指导方针与纲领性文件。2、二级文件:流程性…
-
实验室做风险评估的18个要点
-
实验室做风险评估的18个要点对实验室安全进行风险评估,及时发现安全隐患,采取有效控制措施,尽量避免发生实验室安全事故。实验室应进行风险评估,需要按照下列内容进行评估:1)化学、物理、生物等风险源已知或未知的特性,与环境的交互作用、相关实验数据、过往资料、预防和治疗方案等;2)与实验室本身或相关实验室已发生…

-
搞定清洁验证和确认,该怎么选择…
-
1.分析方法在清洁验证中选择一个合适的分析方法是非常必要的,该适当的分析方法应能够充分检测相关残留物。理解可以从分析结果中得出什么结论也很重要(例如检测的是产品还是清洁剂,结果是否合格?),检测结果决定了清洁方法是否可行或需要进一步改进。本章讨论的内容是怎样选择一个合适的测试方法,包括适用性、化学和微生…

-
干货:偏差变更和验证的误区
-
一个好汉三个帮,流程建设也有三个好帮手,就是偏差、变更和验证,他们都是围绕着标准化这个核心进行的。验证确定标准,变更优化标准,偏差管理确保及时纠正。很多企业在实施的时候,不能理解何谓系统化,忽视各质量活动内在的关联性,于是对以上工作常常执行的片面、孤立。例如验证的归验证,不关注后续标准的可执行性。例如…

-
GMP相关信息:制药偏差OOS&O…
-
OOS和偏差是有区别的。首先OOS属于偏差;其次OOS是一种影响最终产品质量的偏差。以纯化水为例当对纯化水系统进行周期性检查时,若该批次纯化水没有用于生产(仅存储在罐中,不对其它产品产生影响),检查时微生物或理化指标起出内控标准,则称作偏差,不是OOS;若该批次纯化水投入使用了,同步检查过程中发现结果超…

-
317个制药行业常用英语词汇,包含…
-
1、药品生产质量管理规范GMP:Good ManufacturingPractice2、国家食品与药品监督管理局State Food andDrug Administration3、总则GeneralProvisions4、《中华人民共和国药品管理法》the DrugAdministration Law of the Peoples Republic of China5、制剂Preparation6、原料药API: Active PharmaceuticalIngredient7、成品fin…



