法规动向
-
重磅!CDE公开征求《药品说明书和…
-
5月15日,国家药品监督管理局药品审评中心发布了关于公开征求《药品说明书和标签管理规定》(修订稿)意见的通知。公告原文药品说明书是载明药品重要信息的法定文件,现行《药品说明书和标签管理规定》于2006年6月1日起实施。随着新修订的《药品管理法》和《药品注册管理办法》的颁布实施,亟需对《药品说明书和标签管理规定…
-
国家药监局:注射剂一致性评价政…
-
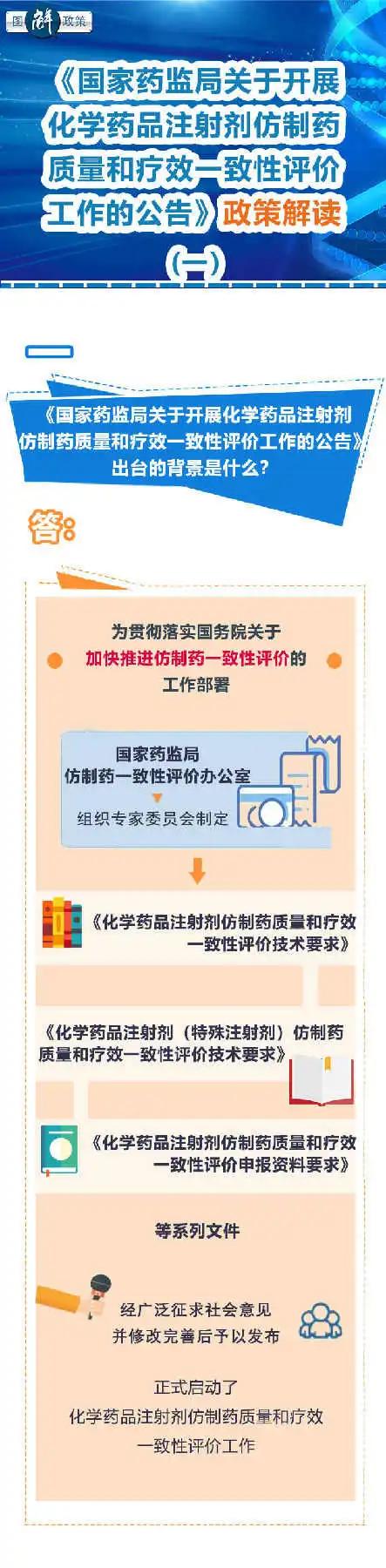
今日,国家药监局发布了《关于开展化学药品注射剂仿制药质量和疗效一致性评价工作的公告》的政策解读,如下
-
重磅!CDE:公开征求《药品说明书…
-
5月15日,国家药品监督管理局药品审评中心发布了关于公开征求《药品说明书和标签管理规定》(修订稿)意见的通知。公告原文药品说明书是载明药品重要信息的法定文件,现行《药品说明书和标签管理规定》于2006年6月1日起实施。随着新修订的《药品管理法》和《药品注册管理办法》的颁布实施,亟需对《药品说明书和标签管理规定…
-
官方解读来了,新版GCP有何变化?…
-
4月29日,国家药监局发布了《药物临床试验质量管理规范》解读。一、《规范》修订的背景新修订的《药物临床试验质量管理规范》(2020年第57号)已于2020年4月23日印发,自7月1日起施行。2003年国家食品药品监督管理局发布施行《药物临床试验质量管理规范》(原局令第3号,简称《规范》),对推动我国临床试验规范研究和提升质…
-
国家药监局发布《GMP 附录-血液制…
-
今日,国家药监局审核查验中心发布了《药品生产质量管理规范血液制品附录》修订草案,如下:为加强对血液制品的监督管理,提高我国血液制品生产企业GMP实施水平,国家药监局组织有关部门对《药品生产质量管理规范血液制品附录》进行了修订,形成征求意见稿(附件),现向社会公开征求意见。请于2020年4月30日前将意见和建议反…

-
2020版药典草案,审议通过!
-
4月13日,国家药监局发布了“第十一届药典委员会执行委员会会议在京召开审议通过2020年版《中国药典》草案”的新闻。新闻稿还透露了2020版药典的增修订情况:2020年版《中国药典》新增品种319种,修订3177种,不再收载10种,品种调整合并4种,共收载品种5911种。l一部中药收载2711种,其中新增117种、修订452种。l二部化学药…



