公司业务
一、FDA GMP认证
FDA(Food and Drug Administration)是美国国会授权的食品和药品管理机构,负责监督和管理食品、药品、医疗器械、化妆品以及其他与公共健康相关的产品。FDA的主要任务是确保公众在使用这些产品时的安全性、有效性和正确标识。
在常见的用法中,"FDA认证"并非FDA官方使用的术语。人们常用"FDA认证"来指代以下三种情况:
FDA注册:对于出口到美国的食品、药品和医疗器械企业,必须在FDA进行注册,包括企业和产品的列名。若未完成注册,海关将不予清关。这是一项强制性要求;
FDA检测:FDA检测通常指的是对食品接触材料的安全检测,产品包装材料的检测,医疗产品的生物相容性测试和临床安全测试等。这些检测旨在确保产品的安全性和符合FDA的相关标准;
FDA批准:FDA批准主要涉及药品领域。当药品经过严格的研究、试验和评估后,获得FDA的批准,才能在美国市场上销售和使用。
二、项目目标
德斯特DST在与企业议定的时间内,帮助企业通过美国FDA认证,帮助企业产品完善进入美国和欧洲市场的法律手续,使企业的产品顺利进入美国市场。中国国内产品在欧、美市场的合法上市将对产品在国内市场及国际其他市场带来积极影响。
三、服务方式
1. 现有质量管理体系差距评估,与FDA法规做比对;
2. 整体设计,了解现有公司结构,生产体系 、QA体系、QC体系、供应链体系、工程体系等等;
3. FDA培训,对公司相关负责人员及员工进行FDA药品通用法规培训;
4. FDA法规专题培训,对公司相关负责人进行FDA药品法规专题培训;
5. 收集公司现有质量文件,进行质量文件系统提升;
6. 质量文件体系推行;
7. 对体系的有效性进行检查;
8. 体系有效性的检查,在FDA来审核之前,安排本公司评审员进行模拟审核;
9. 陪同FDA审厂、翻译;
10. 协助企业对FDA审厂提出的不符合项进行整改直至FDA关闭不符合项。
四、FDA验厂经验分享:
1. 企业生产及出口美国的量越大,用户抱怨越多,被FDA查厂的可能性越大;
2. 但中国(含港澳台)的企业,无论是一类,还是二类,三类,被FDA查厂的概率非常大, 本公司接触到大量低风险产品验厂的案例;
3.所有检查费、机票、差旅、五星酒店、餐费等所有费用均由FDA承担;
4.FDA通常提前1-3个月通知验厂,但不会通知具体到厂日期;
5.通常FDA只来一个人,正常审核4天;
6. 质量手册、程序文件等重要文件需翻译成英文,环境卫生要搞好;
7. FDA更强调内审及记录、相关部门的签字;
8. FDA非常重视法律法规、专业知识、作业指导原则等员工培训与执行、签字;
9. 如有不符合项,审核员会现场开出483表;
10. 审核员提出的所有问题,企业必须在规定时间内提交书面回复,越快越好;
11. 重大不符合项,审核员会现场开出警告信(Warning letter),企业须在规定时间内完成整改。
四、FDA案例
1.浙江某药企FDA项目
2.广东某药企FDA项目
3.四川某药企注射剂FDA项目
4.成都某生物企业原料药FDA项目
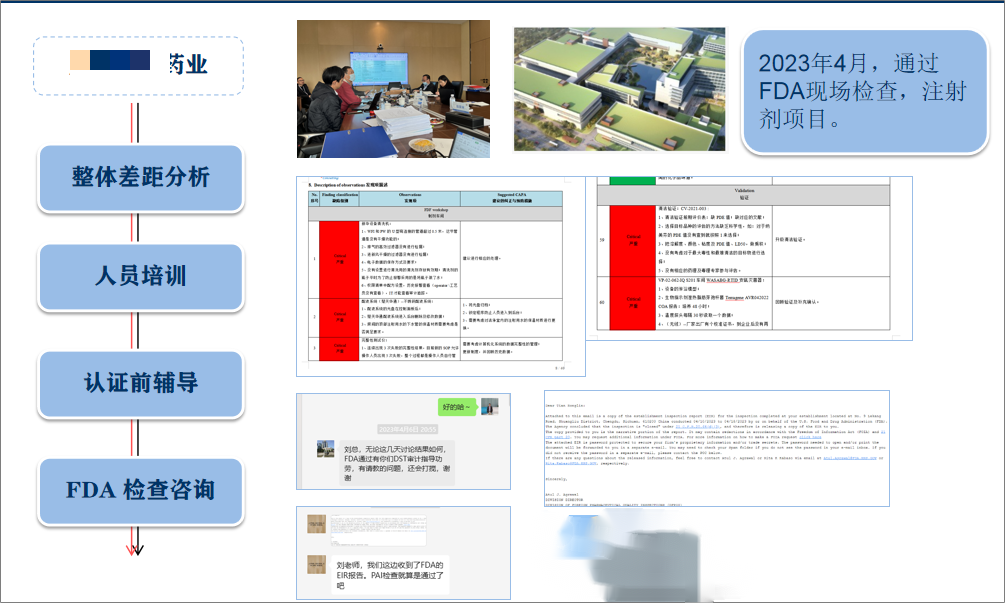
5.湖北某药企无菌制剂FDA项目
6.深圳某知名央企OTC FDA项目
7.福建某药企FDA项目
8.江苏某药企API FDA项目
9.其他FDA项目客户
如有FDA认证相关服务需要,请联系18826007039/13326993435(微信同号)~
上一篇:中国GMP认证
下一篇:PIC/S-GMP认证




 德斯特GMP咨询
德斯特GMP咨询 13427069959
13427069959
